Bir sistemi oluşturan atom ve moleküllerin kinetik (titreşim) ve potansiyel (bağ) enerjilerinin toplamı, iç enerji olarak tanımlanmaktadır. Sistem üzerinde iş yapıldığında ya da sisteme enerji aktarıldığında sistemin iç enerjisinde değişiklik meydana gelir.
Sıcaklık, bir sistemdeki atom ve moleküllerin ortalama kinetik enerjisinin bir göstergesidir, bir enerji değildir. Sıcaklık termometre ile ölçülür ve sıcaklık T sembolü ile gösterilir. Sıcaklığın SIʼdaki birimi kelvindir (K).
Isı; sıcaklıkları farklı, etkileşim hâlindeki iki sistem arasında sıcaklığı yüksek olandan düşük olana doğru, sıcaklığın dengelenmesi için transfer edilen enerjidir. Isı Q sembolü ile gösterilir, SIʼdaki birimi jouledür. Temel ısı birimi olmamasına rağmen genellikle kalori (cal) kullanılmaktadır. İki enerji birimi olan joule ve kalori arasında 1 cal yaklaşık olarak 4, 186 J ‘dür.
Bir sistemin ısısı gibi bir kavram yoktur. Isı, aktarılan enerji olduğu için ancak sistemin aldığı ya da verdiği ısının ölçümü yapılabilir. Bu ölçüm kalorimetre kabı ile yapılır.
“Bir cismin içindeki ısı miktarı” ya da “bir sistemin ısısı” şeklinde bir kavram yoktur. Isı, sıcaklık farkı nedeniyle bir sistemden diğer sisteme aktarılan enerjidir.
Önemli Bilgi
TERMOMETRELER
Termometreler, sıcaklık ölçümünde kullanılan aletlerdir. Termometre seçimi, sıcaklığı ölçülmek istenen madde ya da ortamın ortalama sıcaklığına bağlı olarak seçilir. Bu nedenle termometreler kullanım amaçlarına göre sıvılı, metal (katı) ve gazlı olmak üzere üç çeşittir.
Metal Termometreler
Metallerin genleşme özelliğine bağlı olarak geliştirilmiş bu termometrelerden eritme, pişirme veya kurutma gibi işlemlerin yapıldığı endüstriyel alanlarda ve fırınlarda yararlanılmaktadır.
Maddenin atom ve moleküllerinin kinetik enerjisinin sıfır olarak öngörüldüğü, yani maddenin atom ve moleküllerinin bütün hareketlerinin durduğu varsayılan teorik sıcaklık değerine mutlak sıcaklık adı verilmektedir.
Gazlı Termometreler
Gazların genleşme özelliğine ve basıncına bağlı olarak çalışan bu termometrelerden laboratuvarlarda yararlanılmaktadır.
Sıvılı Termometreler
Sıvılı termometrelerin yapısı temel olarak kılcal cam boru, renklendirilmiş sıvı ve hazneden oluşmaktadır.
Ölçümün hassasiyeti;
• kılcal borulardan genleşme kat sayısı az ve kesit alanı küçük olan boruya,
• renklendirilmiş sıvılardan genleşme katsayısı çok olan sıvıya,
• sıvı haznesinin büyüklüğüne,
• sıcaklık aralığının ölçeklendirilme miktarına bağlıdır.
Mutlak sıcaklık, Kelvin ölçeğinde 0 K ya da Celcius ölçeğinde -273,16 oCʼye karşılık gelmektedir.
Bu sıcaklıktaki bir maddenin atom ve moleküllerinin bütün hareketinin durduğu öngörülmektedir. Maddenin sıcaklığını bu sıcaklık değerinin altına düşürmek mümkün değildir. Sıcaklığı mutlak sıcaklıktan yüksek maddelerin atom ve molekülleri ise hareket hâlindedir. Hareket hâlindeki bu tanecikler birbirleri ile çarpışır ve birbirlerine enerji aktarır.
Sıvılı termometrelerde ölçeklendirme deniz seviyesinde, 1 atm basınç altındaki suyun donma ve kaynama sıcaklıkları arasında yapılır. Sıcaklık ölçeklerine Kelvin (Kelvin), Celcius ve Fahrenheit termometreleri örnek olarak verilebilir.
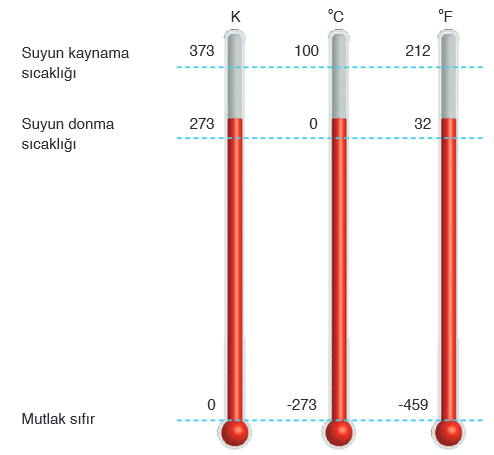
Kelvin termometresinde suyun donma sıcaklığı 273 K, kaynama sıcaklığı ise 373 Kʼdir. Termometre 100 eşit parçaya bölünerek ölçeklendirilmiştir. Celcius termometresinde suyun donma sıcaklığı 0 oC, kaynama sıcaklığı 100 oC olarak belirlenmiştir. Termometre 100 eşit parçaya bölünerek ölçeklendirilmiştir.
Fahrenheit termometresinde ise suyun donma sıcaklığı 32 oF, kaynama sıcaklığı 212 oF alınmış ve termometre 180 eşit parçaya bölünerek ölçeklendirilmiştir. Kelvin, Celcius ve Fahrenheit termometreleri en çok kullanılan termometrelerdir. Bilimsel çalışmalarda Kelvin ölçeklendirmesi kullanılmaktadır. Suyun donma ve kaynama sıcaklığının, ölçeklendirme aralıklarının farklı alındığı başka termometreler de bulunmaktadır.
Aynı ortamdaki termometrelerle aynı sıcaklık ölçülür fakat ölçeklendirme farklı olduğu için termometrelerin üzerinde okunan değerler birbirinden farklı olur. Celcius, Kelvin ve Fahrenheit termometrelerinde okunan değerler sırasıyla oC, K, oF ve herhangi bir termometrede okunan değer X, o termometrede ölçülen suyun donma sıcaklığı TD ve kaynama sıcaklığı TK olmak üzere eşitlik aşağıdaki şekilde olur.
\frac{C}{100}{=}\frac{{F}{-}{32}}{180}{=}\frac{{K}{-}{273}}{100}{=}\frac{{X}{-}{T}_{d}}{{T}_{k}{-}{T}_{d}}Fahrenheit temometresinde okunan 122 oF sıcaklık, Celcius termometresinde kaç oC okunur?
\frac{C}{100}{=}\frac{{F}{-}{32}}{180} \frac{C}{100}{=}\frac{{122}{-}{32}}{180} {C}{=}{50}ÖZ ISI ve ISI SIĞASI
Bir maddenin 1 gramının sıcaklığını 1 oC değiştirmek için maddeye verilmesi ya da maddeden alınması gereken ısı miktarına öz ısı adı verilir. Öz ısı c sembolü ile gösterilir. Birimi cal/goC ya da J/kgoC şeklindedir. Öz ısı, maddeler için ayırt edici bir özelliktir. Madde miktarına bağlı değildir.
Suyun öz ısısı 1 cal/goCʼdir ve 1 gram suyun sıcaklığını 1 oC artırmak için suya 1 cal ısı verilmesi gerektiğini ifade eder.
Öz ısı, ısı alan ya da veren bir maddenin sıcaklığının ne kadar hızlı değiştiğinin bir göstergesidir. Öz ısısı yüksek olan maddelerin sıcaklık değişimi yavaş, düşük olanlarınki daha hızlı gerçekleşir. Bu nedenle denizler karalardan daha geç ısınır ve daha geç soğur.
Isı sığası (kapasitesi) bir maddenin sıcaklığını 1 oC değiştirmek için maddeye verilmesi ya da maddeden alınması gereken ısı miktarıdır. Maddenin cinsine ve miktarına bağlı olan ısı sığası C sembolü ile gösterilir. Isı sığasının matematiksel modeli aşağıdaki gibidir. birimi cal/ oC ya da J/ oCʼdir. Isı sığası, madde miktarına bağlı olduğu için ayırt edici bir özellik değildir.
{C}{=}{m}{.}{c}Kütle ve öz ısısı yüksek olan maddelerin sıcaklığını değiştirmek için maddeye daha fazla ısı verilmesi ya da maddeden daha fazla ısı alınması gerekir.
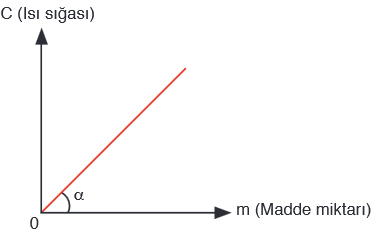
Isı sığasının madde miktarına bağlı değişim grafiği yukarıda verilmiştir. Grafiğin eğimi maddenin öz ısısını verir.
Saf bir madde ısı aldığında ya da bu maddeye ısı verdiğinde (hâl değişimi sıcaklığında olmayan) maddenin sıcaklığı değişir. Sıcaklıktaki bu değişim; ısı miktarına, maddenin kütlesine ve maddenin öz ısısına bağlıdır. Alınan ya da verilen ısı Q, maddenin kütlesi m, öz ısı c ve sıcaklık değişimi ΔT olmak üzere bu nicelikler arasında, Q=m.c.ΔT bağıntısı vardır.





